Fotoserie zur Diagnostik von Influenzaviren
BilderstreckeBildVideo
1 / 13

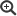
Das Nationale Referenzzentrum (NRZ) für Influenzaviren im Robert Koch-Institut
Im Rahmen der bundesweiten Influenza-Überwachung (auch Surveillance genannt) untersucht das Team des NRZ eingesandte Patientenproben auf Influenzaviren und charakterisiert sie genauestens. Wie viele andere Labore weltweit trägt das NRZ damit auch zur globalen Influenza-Überwachung bei: Die virologischen Daten werden jede Woche an die Weltgesundheitsorganisation übermittelt. Das NRZ untersucht die Proben auch auf andere Viren, die akute Atemwegserkrankungen auslösen, zum Beispiel Rhino- oder Respiratorische Syncytial-Viren (RSV).
Die Aufnahmen dürfen unter Angabe der Quelle (Robert Koch-Institut) für die Berichterstattung und wissenschaftliche Veröffentlichungen verwendet werden. Bei der Online-Berichterstattung ist die Veröffentlichung textbegleitend in Verbindung mit dem Artikel auf Ihrer Internetseite gestattet. Die Quellenangabe muss dabei sichtbar im bzw. am Bild zu sehen sein (Mouseover o.ä. reichen nicht aus). Es ist es nicht gestattet, das Motiv zu verändern, die Datei im eigenen oder einem anderen Internetangebot zum Download anzubieten oder sie weiterzugeben. Nachrichtenagenturen dürfen die Fotos jedoch für Zwecke der Berichterstattung mit Quellenangabe (Robert Koch-Institut) weitergeben.
You may download and use the pictures for news media and scientific publications – please provide the appropriate source (Robert Koch Institute). When using the pictures for online publications, you are allowed to publish them in the context of the respective article on your website. When using the material online, the source must be directly visible (mouse overs or the likes would not be enough). It is not allowed to change the motif, make the pictures downloadable (neither on your own website nor on others) and to redistribute them. However, news agencies may pass on the photos for reporting purposes, provided the source (Robert Koch Institute) is being acknowledged.
nach oben






















