Gonokokken-Resistenzsurveillance (Go-Surv-AMR)
Hintergrund
Infektionen mit Neisseria gonorrhoeae (Gonorrhö) stellen nach aktuellen Schätzungen der WHO weltweit die dritthäufigste sexuell übertragbare Krankheit dar. In Deutschland stehen kaum epidemiologische Daten zur Gonorrhö zur Verfügung, da hierfür bis zum Jahr 2022 keine Meldepflicht bestand. Lediglich im Bundesland Sachsen besteht seit 2001 eine Meldepflicht für den direkten Nachweis von Neisseria gonorrhoeae, wobei sich die dortige Inzidenz zwischen den Jahren 2001 und 2022 vervielfacht hat (LUA Sachsen, Epidemiologischer Wochenbericht 2022/52).
Bei Infektionen mit Neisseria gonorrhoeae kann eine weltweite Ausbreitung von Resistenzen bei für die Behandlung wichtigen Antibiotika beobachtet werden. Um diese besorgniserregende Situation genau zu beobachten und gezielte Gegenmaßnahmen einleiten zu können, wurden sowohl von der Weltgesundheitsorganisation (WHO) als auch vom Europäischen Zentrum zur Prävention und Kontrolle von Krankheiten (ECDC) Aktionspläne entwickelt und Surveillance-Programme ins Leben gerufen. Auch in Deutschland sind Public Health-Maßnahmen zur Gonorrhö ein zentraler Bestandteil der Strategie des Bundesministeriums für Gesundheit zur Eindämmung von HIV, Hepatitis C und B und anderen sexuell übertragbaren Infektionen. Des Weiteren wird Neisseria gonorrhoeae auf der Liste hochpriorisierter, multiresistenter bakterieller Krankheitserreger (PDF, 368 KB, Datei ist nicht barrierefrei) geführt, welche die Grundlage zur Einstufung eines Antibiotikums als Reserveantibiotikum bildet und die entwickelnden Einrichtungen bei der Zulassung einer neuen Substanz von dem Nachweis eines Zusatznutzens befreit.
Antibiotika-Resistenzsurveillance von Neisseria gonorrhoeae in Deutschland
In Deutschland wurde die Antibiotika-Resistenzsurveillance von Neisseria gonorrhoeae im Jahr 2013 als Kooperation zwischen dem Robert Koch-Institut, dem Konsiliarlabor für Gonokokken und einem deutschlandweiten Labornetzwerk ins Leben gerufen (GORENET-Projekt). Seit Januar 2021 wird diese probenbasierte, phänotypische und genotypische Resistenzsurveillance zusammen mit der Meldepflicht für Nachweise von Neisseria gonorrhoeae nach §7.3 des Infektionsschutzgesetzes unter dem Namen Go-Surv-AMR als Amtsaufgabe des RKI weitergeführt.
Ausgewählte, am Go-Surv-AMR teilnehmenden Labore aus ganz Deutschland senden regelmäßig Gonokokken-Isolate zusammen mit dazugehörigen pseudonymisierten epidemiologischen und klinischen Daten an das RKI. Am RKI werden die Proben zentral auf ihre Antibiotikaempfindlichkeit nachgetestet. Hiermit werden aktuelle Entwicklungen der Antibiotika-Resistenz bei Gonokokken-Infektionen in Deutschland kontinuierlich erfasst. Des Weiteren wird die DNA der eingesendeten Proben extrahiert und mittels molekularer Methoden wie beispielsweise der Ganzgenomsequenzierung charakterisiert, um Resistenzdeterminanten zu identifizieren und Genogruppen deutschlandweit aber auch innerhalb Europas und weltweit miteinander vergleichen zu können. Diese Daten und Analysen helfen z.B. dabei, molekulargenetische Unterschiede zwischen resistenten und nicht-resistenten Gonokokken-Stämmen zu identifizieren und auf dieser Basis Therapie-Empfehlungen zu optimieren.
Ergebnisse
Das Antibiotikum Ceftriaxon, das laut Leitlinie als Erstlinien-Therapeutikum bei adhärenten Patienten eingesetzt werden sollte, befindet sich seit einigen Jahren stabil auf sehr niedrigem Resistenzlevel mit unter 1% resistenter Isolate (Abb. 1A). Bei Cefixim, das aktuell als Ersatz für Ceftriaxon gegeben werden kann, bewegt sich der Anteil resistenter Isolate zwischen 1% und 2%.
In den letzten Jahren zeigte sich eine besorgniserregende Entwicklung für das Makrolid-Antibiotikum Azithromycin, welches in der dualen Therapie gemeinsam mit Ceftriaxon oder Cefixim als Erstlinien-Therapeutikum bei nicht sicher adhärenten Patienten empfohlen wird. Während im Jahr 2014 nach aktuell gültigem Standard des Europäischen Komitees für Antimikrobielle Empfindlichkeitstestung (EUCAST, Interpretationsstandard Version 14.0) ca. 1% aller Isolate eine verminderte Empfindlichkeit gegenüber Azithromycin aufwiesen (minimale Hemmkonzentration >1 mg/L), waren dies im Jahr 2022 bereits 24,8% (Abb. 1A). Im Jahr 2023 stieg der Anteil der Isolate mit verminderter Empfindlichkeit gegenüber Azithromycin erstmals seit 2017 nicht weiter an, sondern blieb stabil auf hohem Niveau (2023: 24,6%).
Die früher häufig zur Behandlung der Gonorrhö eingesetzten Antibiotika Penicillin und Ciprofloxacin wiesen beide einen sehr hohen Resistenz-Anteil auf (Abbildung 1B). Im Jahr 2023 waren über 95,4% der Isolate resistent gegenüber dem Antibiotikum Tetracyclin.
 Abb. 1A: Entwicklung der Resistenz von Neisseria gonorrhoeae in Deutschland gegenüber den therapeutisch wichtigen Antibiotika Azithromycin, Cefixim und Ceftriaxon, 2014-2023. *Für Azithromycin wurde ein epidemiologischer Grenzwert herangezogen (Bewertungskriterien nach EUCAST 14.0) Quelle: Go-Surv-AMR
Abb. 1A: Entwicklung der Resistenz von Neisseria gonorrhoeae in Deutschland gegenüber den therapeutisch wichtigen Antibiotika Azithromycin, Cefixim und Ceftriaxon, 2014-2023. *Für Azithromycin wurde ein epidemiologischer Grenzwert herangezogen (Bewertungskriterien nach EUCAST 14.0) Quelle: Go-Surv-AMR
 Abb. 1B: Resistenz von Neisseria gonorrhoeae in Deutschland gegenüber sechs wichtigen Antibiotika, 2018-2023 (Bewertungskriterien nach EUCAST 14.0). *keine Daten für Tetracyclin in 2019. **keine Daten für Penicillin in 2021. Quelle: Go-Surv-AMR
Abb. 1B: Resistenz von Neisseria gonorrhoeae in Deutschland gegenüber sechs wichtigen Antibiotika, 2018-2023 (Bewertungskriterien nach EUCAST 14.0). *keine Daten für Tetracyclin in 2019. **keine Daten für Penicillin in 2021. Quelle: Go-Surv-AMR
Da es sich bei Neisseria gonorrhoeae um einen genetisch hochvariablen Erreger handelt, wurden im Rahmen von molekulargenetischen Analysen in den letzten Jahren für Deutschland eine Vielzahl verschiedener genetischen Gruppen, sogenannten Genogruppen, identifiziert.
Für einige dieser Genogruppen konnten auch genetische Determinanten identifiziert werden, welche mit phänotypischer Antibiotikaresistenz in Verbindung gebracht wurden. So wurde beispielsweise eine Gruppe von aus Deutschland stammenden Isolaten mit verminderter Empfindlichkeit gegenüber dem Cephalosporin Cefixim als neue Genogruppe G10577 beschrieben.
Durch die Überlagerung von Werten der phänotypischen Antibiotikaempfindlichkeit mit genotypischen Stammbäumen konnten in den letzten Jahren mehrere Gruppen nahe miteinander verwandter Isolate, sogenannte Kladen, gemeinsam eingeordnet werden (Abb. 2). Aus Abbildung 2 wird ersichtlich, dass sich mehrere dieser Kladen hinsichtlich ihrer Assoziation mit verminderter Antibiotikaempfindlichkeit gegenüber den therapeutisch relevanten Substanzen Azithromycin, Cefixim und Ceftriaxon abheben.
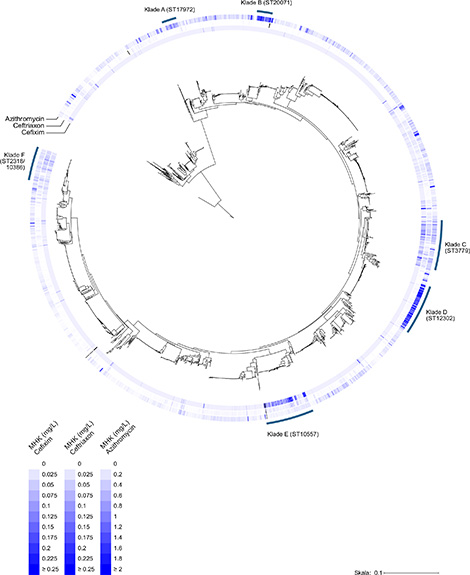
 Abb. 2: Überlagerung der minimalen Hemmkonzentrationen (MHK) mit Dendrogramm der typisierten Neisseria gonorrhoeae Isolate 2016-2020. Quelle: Go-Surv-AMR
Abb. 2: Überlagerung der minimalen Hemmkonzentrationen (MHK) mit Dendrogramm der typisierten Neisseria gonorrhoeae Isolate 2016-2020. Quelle: Go-Surv-AMR
Detailliertere Ergebnisse hierzu enthalten die Projektberichte bzw. wissenschaftliche Veröffentlichungen (siehe Publikationsliste).
Wir freuen uns sehr, wenn Ihr Labor Interesse an einer aktiven Teilnahme an Go-Surv-AMR hat. Nehmen Sie hierzu gerne unkompliziert Kontakt mit uns auf: gosurv@rki.de
nach oben









